حلالیت خاصیت یک ماده برای حل در آب یا یک حلال دیگر است. هر دو مواد جامد و مایع و گاز می توانند در آب حل شوند. با حلالیت ، همه مواد به سه گروه تقسیم می شوند:
- بسیار محلول است
- کمی محلول است
- نامحلول
مواد کاملاً نامحلول وجود ندارد ، بنابراین نام نامحلول مشروط است و باید "عملاً نامحلول" را بخوانید.
حلالیت مواد به درجه حرارت بستگی به دما و فشار دارد ، به عنوان مثال ، ماده KNO3 (نیترات پتاسیم) در دمای + 20 درجه سانتیگراد دارای محلول حلالیت 31.6 گرم در 100 گرم آب و در دمای + 100 درجه سانتیگراد - 245 گرم در 100 گرم آب است.
حلالیت ، رسوب و هیدرولیز نمکها در شرایط عادی

توضیحات مربوط به جدول:
- پ - نمک محلول است (بیش از 0.1 مول در لیتر) ،
- M - نمک کم محلول (0.1-0.001 mol / l) ،
- N - نمک نامحلول (کمتر از 0.001 مول در لیتر) ،
- [H] - هیدرولیز برگشت ناپذیر ، نمک از محلول رسوب نمی کند ، نمک اصلی با انتشار دی اکسید کربن رسوب می کند ، Cr2س3 - رسوب Cr (OH)3 با انتشار سولفید هیدروژن ،
- + - نمک کاملاً با آب واکنش نشان می دهد ،
- - - وجود ندارد،
- * P - توسط کاتیون هیدرولیز می شود ،
- P * - توسط آنیون هیدرولیز می شود.
حلالیت نمک
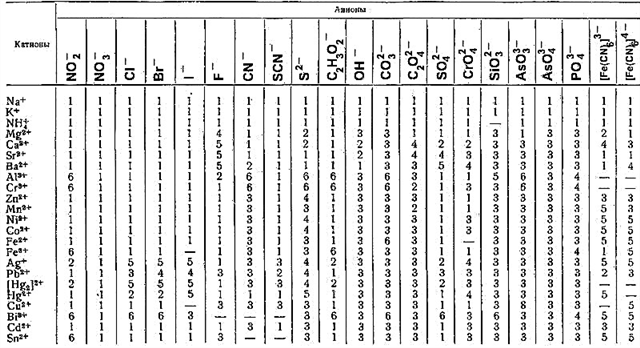
توضیحات مربوط به جدول
- 1 - نمک در آب محلول است ،
- 2 - کمی محلول در آب ،
- 3 - در آب نامحلول ، اما در اسیدهای آلی و معدنی محلول است ،
- 4 - نامحلول در آب و اسیدهای آلی ، اما در اسیدهای معدنی محلول هستند ،
- 5 - نمک در آب و اسیدها محلول نیست.
- 6 - هیدرولیز می شود.
اگر سایت را دوست داشتید ، از محبوبیت آن سپاسگزار خواهیم بود :) در مورد انجمن ، وبلاگ ، انجمن ، درباره ما درمورد ما بگویید. این دکمه ماست:
دکمه کد: